一、PEP的历史
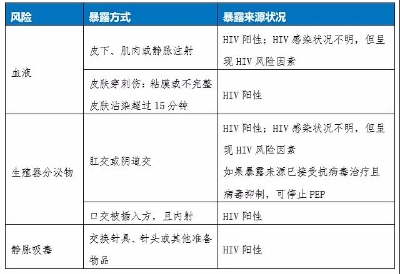
暴露后预防(Post-exposure prophylaxis, PEP)早在十九世纪90年代就开始用于职业暴露处理。美国疾病预防控制中心(USCDC)和世界卫生组织(WHO)分别在2005年和2007年发布了PEP指南。 本文针对WHO、中国、美国和欧洲关于PEP的最新指南,或者艾滋病治疗指南中关于PEP的内容进行了梳理和总结,讨论PEP应用于艾滋病预防的相关场景和标准。本文涉及的指南文本包括: 2016, WHO, “Consolidated Guidelines on the Use of Antiretroviral Drugs for Treating and Preventing HIV Infection” 2016, USCDC, “Updated Guidelines for Antiretroviral Postexposure Prophylaxis After Sexual, Injection Drug Use, or Other Nonoccupational Exposure to HIV—United States, 2016” 2018,中华医学会感染病学分会艾滋病丙型肝炎学组、中国疾病预防控制中心,《中国艾滋病诊疗指南(2018版)》 2020, New York State Department of Health AIDS Institute, “PEP to Prevention HIV” 2020, European AIDS Clinical Society (EACS), “Guidelines (version 10.1)” 二、暴露风险评估 如果出现下列两种情况之一,则不适用PEP: 1)自己已经感染HIV; 2)对方明确是HIV阴性。 如果以上两点均不满足,或无法确定,则需要从两方面的考虑此次暴露的风险性: 一是暴露接触的体液类型。 WHO(2016)指南中罗列了可能造成艾滋病传播的体液,主要包括血液、带血的唾液、乳汁、生殖器分泌物,以及脑脊液、关节液、心包积液、羊水、腹水、胸水等。中国指南(2018)则认为脑脊液、关节液、心包积液、羊水、腹水、胸水具有传染性,但其引起感染的危险程度尚不明确。 二是暴露的方式。 风险较高的暴露方式主要包括:1)粘膜(例如性接触,溅到眼睛、鼻子或口腔等)和2)注射或穿刺(例如输血、针刺等)。 EACS(2020)指南中详细说明可能造成HIV感染的暴露方式,其中值得注意的是在“皮肤穿刺伤”部分,明确说明是“粘膜或不完整皮肤沾染(体液)超过15分钟”才需要考虑暴露后预防。
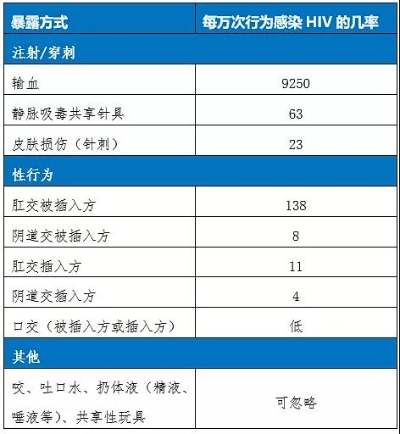
USCDC则明确列出了单次行为感染HIV的风险,有助于具体评估被暴露者的感染风险,从而决定是否推荐使用PEP。
中国指南(2018)指出:如暴露源为HIV感染者的血液,那么经皮肤损伤暴露感染HIV的危险性为0.3%,经黏膜暴露为0.09%,经不完整皮肤暴露的危险度尚不明确,一般认为比黏膜暴露低。
三、PEP方案 PEP治疗方案目前都是推荐使用三种药物联合使用,其中骨干药物较为明确,一般推荐替诺福韦(TDF)+拉米夫定(3TC)或恩曲他滨(FTC),包括TDF/FTC或TDF/3TC合剂。EACS(2020)的指南增加了丙酚替诺福韦(TAF),但纽约卫生局(2020)则没有纳入TAF,主要因为研究发现TAF在“阴道、宫颈、直肠中的药物浓度(较TDF)更低”。USCDC和中国CDC针对肾功能受损者,推荐齐多夫定(AZT)+拉米夫定(3TC),但纽约卫生局(2020)已经明确不再推荐AZT用于PEP。 第三种药物的选择则体现出了较大的多样性: WHO(2016)首推的是洛匹那韦/利托那韦(LPV/r,克力芝™)或阿扎那韦(ATV);替代方案为拉替拉韦(RAL,艾生特™)、达卢那韦/利托那韦(DRV/r)或依非韦仑(EFV)。其中依非韦仑因为可能导致早期的神经精神倒错,不建议有焦虑情绪的人使用。 USCDC(2016)和纽约卫生局(2020)首推拉替拉韦(RAL,艾生特™)或多替拉韦(DTG,特威凯™);替代方案为达卢那韦/利托那韦(DRV/r)。纽约卫生局(2020)的替代方案还包括阿扎那韦(ATV)或福沙那韦/利托那韦(FPV/r)。 EACS(2020)首推拉替拉韦(RAL,艾生特™)或达卢那韦/利托那韦(DRV/r);替代方案包括多替拉韦(DTG,特威凯™)或必妥维(TAF/FTC/BIC)合剂。 中国指南(2018)首推拉替拉韦(RAL,艾生特™)或其他INSTIs;替代方案为洛匹那韦/利托那韦(LPV/r,克力芝™)或达卢那韦/利托那韦(DRV/r)。 合剂方面,EACS(2020)推荐必妥维(TAF/FTC/BIC)三合一合剂作为备选方案;纽约卫生局(2020)推荐Stribild(EVG/COBI/FTC/TDF)四合一合剂备选。 另外,其他创新药物在PEP应用中具有广泛前景,例如已经批准上市的艾博韦泰(ABT)是一种长效HIV融合抑制剂,作用于病毒进入细胞的初始环节,阻断病毒进入细胞,用药后72秒迅速达到血药峰值,半衰期长达12天,安全性好,具有暴露后预防用药的优势。 四、PEP管理和随访 1、使用前的检查和评估: USCDC(2016)在这方面的规定最为详尽,所有人都需要做HIV、乙肝(表面抗体、表面抗原、核心抗体)和丙肝检测;对经性暴露的人,还需要做性病检测(包括梅毒、淋病、衣原体)和孕检;对采用TDF/FTC+RAL或DTG方案的人,还需要额外做肌酐和转氨酶检测。EACS(2020)只规定做HIV、乙肝、丙肝和孕检,但要求在暴露后48小时内。 WHO(2016)专门提及了对于乙肝病毒携带者,需严格监控PEP停止后是否发生乙肝病毒爆发。USCDC(2016)将范围明确限定在活跃的乙肝病毒携带者(即乙肝表面抗原[HBsAg]阳性)。 2、咨询和随访: USCDC(2016)要求在48小时内进行回访,了解是否获得PEP药物,评估药物耐受度和服药依从性;并在第2周再进行一次回访,确保药物获得并了解服药副作用。WHO(2016)也建议为PEP使用者提供依从性强化咨询。 EACS(2020)建议PEP结束时及结束一个月各做1次HIV检测。中国指南(2018)则建议发生HIV职业暴露后立即、4周、8周、12周和6个月后各检测1次HIV 抗体。